


VITA E CONTRIBUTI ALLA SCIENZA
Sir Joseph John Thomson fisico inglese nacque a Cheetham Hill (Manchester) nel 1856 e moŕ a Cambridge nel 1940).
Allievo di Maxwell a Cambridge, nel 1884 fu nominato professore di fisica sperimentale e, grazie al suo contributo il laboratorio Cavendish, in cui lavoṛ per quarantadue anni e di cui più tardi fu direttore, divenne una delle principali scuole di fisica sperimentale del mondo. Fu professore all'Istituto reale di Londra (1905) l'anno successivo gli fu conferito il premio Nobel per la fisica. Nel 1916 divenne presidente della Royal Society e nel 1919 fu eletto socio straniero dell'Accademia delle scienze di Francia.
Thomson si interesṣ a tutti i problemi della fisica in generale, ma soprattutto dedic̣ le proprie ricerche all'indagine delle proprietà elettriche della materia. Nel 1894 misuṛ la velocità dei raggi catodici; nel 1897, con una celebre esperienza, determiṇ il rapporto e/m tra la carica e la massa dell'elettrone e nell'anno successivo ottenne il valore assoluto della carica stessa che dimostṛ essere uguale e contraria a quella dello ione idrogeno, deducendo che la massa degli elettroni è molto più piccola di quella del più leggero atomo conosciuto. Nel compiere queste ricerche elaboṛ una tecnica sperimentale che, ripresa da F. W. Aston, condusse alla costruzione dello spettrografo di massa, che permise di pesare gli atomi e porṭ poi alla scoperta degli isotopi. Propose un modello atomico in cui gli elettroni erano incorporati in una sfera carica positivamente e soggetti a moto armonico.
LA DETERMINAZIONE DELLA CARICA SPECIFICA DELL'ELETTRONE
Thomson idẹ un esperimento per determinare la carica specifica dell'elettrone i cui punti fondamentali possono coś essere rassunti:
Thomson prese in considerazione un fascio di raggi catodici omogenei: supponendo che ogni particella abbia carica e e indicando con N il numero di particelle che passano attraverso una sezione del fascio in un dato tempo, si pụ concludere che la quantità di carica totale Q trasportata dal fascio risulterà:
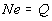
Il valore di Q pụ essere ottenuto per via sperimentale se i raggi vengono immessi in una campana di vetro collegata ad un elettrometro.
Quando i raggi catodici investono un corpo solido la temperatura del corpo aumenta; l'energia cinetica delle particelle, dunque, viene convertita in calore: se si suppone che tutta l'energia cinetica venga trasformata in calore, riuscendo a misurare l'incremento di temperatura di un corpo di nota capacità termica, sarà possibile determinare l'energia cinetica (K) delle particelle; per cui detta v la velocità di una singola particella:
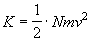
In presenza di un campo magnetico B uniforme il fascio elettronico devia per cui detto r è il raggio di curvatura del cammino dei raggi allora:
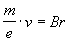
Per cui
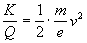
Utilizzando le relazioni individuate e, chiamando I il prodotto Br, si possono determinare sia la velocità delle particelle sia la loro carica specifica, che risultano
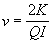
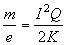
Thomson riusć a determinare con una serie di esperimenti i valori di K, I e Q e, pertanto, riusć a determinare il valore di m/e constatando che questo risultava indipendente si a dalla natura del gas contenuto nel tubo sia dal materiale di cui era costituito il catodo.