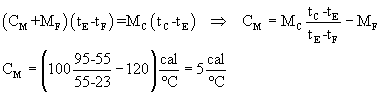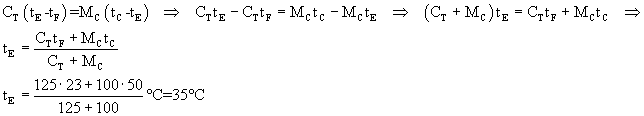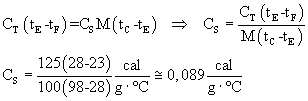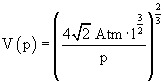Quesito 1
Un recipiente con pareti adiabatiche contiene inizialmente 120 g di acqua alla
temperatura di 23°C in equilibrio termico con il recipiente stesso.
Nel recipiente vengono immessi 100 g di acqua alla temperatura di 95°C e, dopo un tempo
adeguato, si può stimare che tutto il sistema raggiunga una temperatura di equilibrio di 55°C.
Attribuendo all'acqua un calore specifico di 1 cal/g °C
- calcolare la capacità termica media del recipiente;
- calcolare quale sarebbe risultata la temperatura di equilibrio del sistema se l'acqua
calda immessa fosse stata alla temperatura di 50°C.
Nel recipiente, nelle condizioni iniziali date, viene immesso un corpo omogeneo di
massa Mc=100 g alla temperatura tc= 98°C e, dopo un tempo adeguato,
il sistema raggiunge una temperatura di equilibrio te=28°C.
- Calcolare il calore specifico della sostanza di cui è composto il corpo.
Svolgimento
Quesito 2
Un decimo di mole di gas perfetto biatomico inizialmente nello stato A a pressione PA=2 Atm
e volume VA=2 l viene fatto espandere reversibilmente con una trasformazione di
equazione pV x=cost fino ad uno stato C con volume VC=8 l e
pressione PC=0.25 Atm.
- Calcolare il valore dell'esponente x.
- Calcolare il valore del volume VB assunto dal gas quando passa per lo stato B in cui la pressione è PB=1 Atm.
- Calcolare il lavoro effettuato dal gas nella trasformazione dallo stato A allo stato C.
- Calcolare quanto calore bisogna fornire al gas per portarlo con una trasformazione
isobara ad uno stato D di temperatura uguale a quella dello stato iniziale A.
Svolgimento
Svolgimento del quesito 1
-
Dato che il calore specifico dell'acqua è 1 cal/g °C, la capacità termica dell'acqua
fresca contenuta nel recipiente, nelle unità di misura adottate nel testo, coincide numericamente
con la massa MF di quest'acqua. Indicando com CM la capacità termica
media del recipiente, il sistema recipiente+acqua fresca ha capacità termica totale
CT=CM+MF
e il calore QA assorbito dal sistema nel passaggio dalla
temperatura iniziale a quella di equilibrio risulta
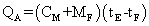
Il calore QC ceduto dalla massa MC di acqua calda risulta, in modulo,
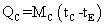
Uguagliando i due valori assoluti si ha
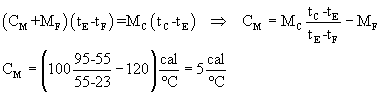
La capacità termica totale CT di recipiente e acqua fresca contenuta è 125 cal/°C.
-
Immettendo nel recipiente contenente acqua fresca (23°C) dell'acqua meno calda della
precedente (50°C),
conoscendo la capacità termica totale CT (calcolata al punto precedente),
l'uguaglianza tra i calori scambiati risulta
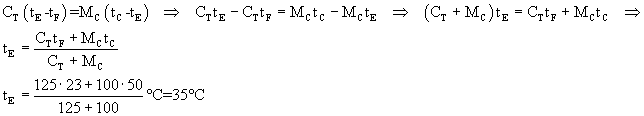
-
Immettendo nel recipiente contenente acqua fresca (23°C) un corpo omogeneo caldo (98°C),
conoscendo la capacità termica totale CT e indicando con CS il calore specifico
della sostanza di cui è composto il corpo, l'uguaglianza tra i calori scambiati risulta
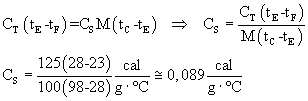
Svolgimento del quesito 2
-
Uguagliando i valori del prodotto della pressione per la potenza del volume nello
stato A e nello stato C si ottiene
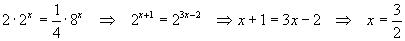
-
Noto l'esponente, il valore della costante dell'equazione della trasformazione si ricava attribuendo a
pressione e volume i valori assunti nello stato A (o nello stato C)
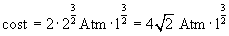
Quindi l'equazione della trasformazione è
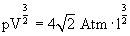
Esprimendo il volume in funzione della pressione si ha
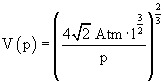
e quindi
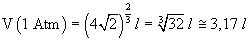
-
Esprimendo la pressione in atmosfere in funzione del volume in litri si ha
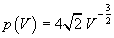
Il lavoro, in litri per atmosfere, si ottiene dall'integrale
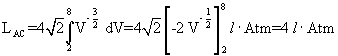
-
Il calore assorbito in una trasformazione isobara per un g.p. biatomico a molecole "rigide"
è dato da
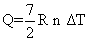
Dall'equazione di stato dei g.p. per molecole biatomiche "rigide" si ha inoltre
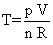
e la variazione di temperatura dallo stato C allo stato D è quindi
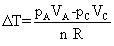
Sostituendo questa espressione di ΔT nell'espressione di Q si ha
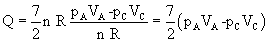
Con i valori di pressione e volume negli stati A e C si ottiene
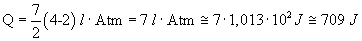
![]()
![]()